
Composition
Principes actifs
Dexamethasoni dihydrogenophosphas ut Dexamethasoni natrii phosphas.
Excipients
Dexaméthasone Galepharm Amp 4 mg/1 ml
Propylenglycolum (E 1520) 20 mg, Natrii chloridum, Dinatrii edetas, Natrii hydroxidum, Aqua ad iniectabilia q.s. ad solutionem pro 1 ml, corresp. 3.7 mg Natrium.
Dexaméthasone Galepharm Amp 8 mg/2 ml
Propylenglycolum (E 1520) 40 mg, Natrii chloridum, Dinatrii edetas, Natrii hydroxidum, Aqua ad iniectabilia q.s. ad solutionem pro 2 ml, corresp. 7.4 mg Natrium.
Forme pharmaceutique et quantité de principe actif par unité
1 ampoule Dexaméthasone Galepharm Amp 4 mg/1 ml contient 4 mg de dexamethasoni dihydrogenophosphas correspondant à 3.32 mg de dexaméthasone.
1 ampoule Dexaméthasone Galepharm Amp 8 mg/2 ml contient 8 mg de dexamethasoni dihydrogenophosphas correspondant à 6.64 mg de dexaméthasone.
Indications/Possibilités d’emploi
Administration systémique
Œdème cérébral (provoqué par: tumeur cérébrale, traumatisme cranio-cérébral, hémorragie intracérébrale, interventions neurochirurgicales, abcès cérébral, apoplexie, encéphalite, méningite, radiolésions). Choc anaphylactique (après injection initiale d’adrénaline). Choc polytraumatique (prophylaxie du poumon de choc et de l’embolie graisseuse). Etat de mal asthmatique. Poussées aiguës de dermatoses sévères (p.ex. œdème de Quincke, pemphigus vulgaire, eczémas non contrôlables, sarcoïdose cutanée). Hémopathies aiguës (p.ex. anémie hémolytique aiguë). Insuffisance corticosurrénalienne primaire et secondaire aiguë (toutefois uniquement lors de traitement concomitant par un minéralocorticoïde). Prophylaxie et traitement des vomissements induits par des cytostatiques.
Traitement de la maladie à Coronavirus 2019 (COVID-19) chez les adultes et les adolescents (âgés d’au moins 12 ans et ayant un poids corporel d’au moins 40 kg) qui nécessitent un apport d’oxygène supplémentaire.
Administration locale
Traitement péri-articulaire et par infiltration, p.ex. en cas de: périarthrite scapulo-humérale, épicondylite, bursite et tendovaginite. Injection intra-articulaire, p.ex. en cas d’arthrite rhumatismale si des articulations isolées sont atteintes ou ne réagissent qu’insuffisamment à un traitement général, et en cas d’arthrose déformante (réaction inflammatoire associée).
Posologie/Mode d’emploi
L’administration parentérale de glucocorticoïdes ne doit être réservée qu’aux situations d’urgence et aux situations dans lesquelles un traitement par voie orale est impossible ou non souhaité.
Instructions générales pour la posologie
La dexaméthasone est administrée selon une posologie individuelle tenant compte de la gravité et de l’évolution de la maladie, de la réaction du patient ainsi que de la durée probable du traitement. Il convient aussi de déterminer si un traitement quotidien ou un traitement intermittent est approprié. D’éventuelles complications dépendent à la fois de la posologie et de la durée de traitement.
L’effet maximal de la dexaméthasone, comme celui de tous les glucocorticoïdes, ne se manifestant qu’après un certain délai (1 à 2 heures), la préparation ne doit jamais être administrée dans des situations menaçant la vie du patient (p.ex. état de mal asthmatique, œdème cérébral aigu) sans traitement supplémentaire à effet immédiat.
Dès que cette phase aiguë est maîtrisée, une posologie parentérale initiale élevée doit être diminuée progressivement et remplacée par une administration orale.
En cas d’absence d’amélioration au bout de quelques jours, l’administration parentérale de glucocorticoïdes ne doit pas être poursuivie.
Un traitement à long terme ne devrait être entrepris qu’après une évaluation soigneuse des bénéfices par rapport aux risques. Lors de traitement à long terme, l’apparition de signes nécessitant une réduction de la posologie ou une interruption de la médication doit être attentivement surveillée.
Comme toute glucocorticothérapie, le traitement par Dexaméthasone Galepharm ne doit pas être interrompu soudainement, mais en réduisant la dose journalière lentement et progressivement afin d’éviter une aggravation ou une reprise aiguë de la maladie, une insuffisance corticosurrénalienne aiguë et un syndrome de sevrage de la cortisone.
Dans le cas où Dexaméthasone Galepharm doit remplacer d’autres glucocorticoïdes, les doses d’équivalence doivent être prises en considération (voir «Propriétés/Effets»).
Administration systémique
En cas de formes aiguës d’œdème cérébral, p.ex. à la suite de lésions crânio-cérébrales, d’hémorragies intracérébrales et d’accidents vasculaires cérébraux: administrer la dose initiale de 40 à 100 mg i.v.; après 2 à 4 jours, 4 à 8 mg i.v. ou i.m. à intervalle de 2 à 4 heures durant 5 à 8 jours.
En cas de formes subaiguës ou chroniques d’œdèmes cérébraux, p.ex. lors de tumeurs cérébrales, d’abcès cérébraux, de méningo-encéphalites et de radiolésions: administrer une dose initiale de 8 à 12 mg i.v.; poursuivre le traitement à raison de 4 mg i.v. ou i.m. à 6 heures d’intervalle.
Pour le traitement initial du choc anaphylactique (après injection initiale d’adrénaline) ainsi que du choc occasionné par des lésions multiples (prophylaxie du poumon de choc ou de l’embolie graisseuse): administrer 40 à 200 mg i.v.. Dans les cas graves, soit répéter la dose initiale au bout de 4 à 12 heures, soit administrer 16 à 40 mg i.v. toutes les 6 heures durant 2 à 3 jours.
En cas d’état de mal asthmatique: administrer une dose initiale de 40 à 80 mg i.v.; selon la gravité du cas, répéter la dose initiale 3 à 6 heures plus tard et poursuivre le traitement par 4 mg i.v. par jour et, le cas échéant, passer au traitement par voie orale.
En cas de dermatoses aiguës et d’hémopathies aiguës: administrer une dose initiale de 16 à 40 mg i.v. et poursuivre le traitement par voie orale.
Pour le traitement de l’insuffisance corticosurrénale aiguë (crise d’Addison): initier le traitement avec 8 à 16 mg i.v. (toutefois uniquement lors de traitement concomitant par un minéralocorticoïde).
Pour la prophylaxie et le traitement des vomissements induits par des cytostatiques: administrer une ampoule de 8 mg i.v. la veille du traitement, 8 à 12 mg i.v. au début du traitement, puis 4 mg i.v. toutes les 4 à 6 heures durant au moins 48 heures.
Pour le traitement de la COVID-19, les patients adultes reçoivent 6 mg par voie intraveineuse une fois par jour durant une période allant jusqu’à 10 jours. La durée du traitement dépend de la réponse clinique et des besoins individuels du patient.
Administration locale
Pour un traitement péri-articulaire et intra-articulaire ou par infiltration locale dans des conditions d’asepsie strictes: injecter 4 ou 8 mg. Lors d’une injection dans une très petite articulation, 2 mg suffisent. En fonction de la gravité de l’affection, le nombre d’infiltrations ou d’injections ne doit pas dépasser 3 à 4 par articulation. L’intervalle entre les injections ne doit pas être inférieur à 3 à 4 semaines.
Traitement à long terme
Un traitement à long terme de plus de 2 semaines peut, en inhibant la libération d’ACTH, conduire à une insuffisance corticosurrénalienne pouvant aller jusqu’à l’atrophie des glandes corticosurrénales. Cette perte de fonction corticosurrénalienne peut durer une année ou plus et constitue un risque de mise en danger de la vie du patient dans des situations de stress et de surmenage.
Le trouble de la réaction au stress sous glucocorticothérapie à long terme exige une adaptation des doses de corticoïdes aux conditions de stress. Pour cela, l’hydrocortisone i.v. est habituellement utilisée:
- en cas de maladies générales: doubler ou éventuellement tripler la dernière dose de dexaméthasone
- en cas d’interventions légères: administrer 100 mg d’hydrocortisone i.v. de plus avant l’intervention
- en cas d’interventions d’importance moyenne: administrer en plus 100 mg d’hydrocortisone par voie i.v. avant l’opération et, ensuite, 100 mg d’hydrocortisone toutes les 6 heures durant 24 heures
- en cas d’interventions chirurgicales importantes: administrer en plus 100 mg d’hydrocortisone avant le début de l’opération et, ensuite, toutes les 6 heures durant au moins 72 heures. Poursuivre le traitement en fonction de l’évolution
Mode d’administration correct
Les ampoules de Dexaméthasone Galepharm sont injectées par voie intraveineuse, intramusculaire, intra-articulaire ou par infiltration locale.
Les infiltrations locales et les injections intra-articulaires doivent être effectuées dans des conditions d’asepsie rigoureuses. La peau doit être préparée en vue de l’opération (rasage éventuel, dégraissage, alcool, badigeonnage à l’iode). Eviter les injections dans les tendons.
Instructions posologiques particulières
Enfants et adolescents
La posologie doit être ajustée en fonction de la gravité de la maladie et de la réponse au traitement plutôt qu’en fonction de l’âge, du poids ou de la taille de l’enfant. Chez les enfants en bas âge et les enfants âgés de 0 à 11 ans, des doses plus faibles que celles administrées aux adultes sont généralement suffisantes. En cas de réponse suffisante du patient, la dose de dexaméthasone doit être réduite par petits paliers à la dose la plus faible possible et le traitement interrompu aussitôt que possible.
Administration i.v.
- Œdème cérébral déclenché p.ex. par:
- tumeur cérébrale: administrer une dose initiale de 0.5 à 1 mg/kg, puis 0.25 à 0.5 mg/kg par jour en 4 fois
- intervention neurochirurgicale: administrer 1 mg/kg en phase préopératoire, puis 0.2 mg/kg toutes les 4 heures pendant 24 heures
- encéphalite/méningite: administrer 0.15 mg/kg toutes les 6 heures durant 4 jours, ou 0.4 mg/kg toutes les 12 heures durant 2 jours, en commençant avant la première antibiothérapie
- choc anaphylactique (après injection initiale d’adrénaline): dose initiale: 7.5 à 15 mg chez les nourrissons, 4.5 mg/kg chez les enfants plus âgés; 2e jour: réduire la dose à la moitié de la dose initiale; 3e jour: réduire la dose à un quart de la dose initiale
- choc polytraumatique (prophylaxie du poumon de choc et de l’embolie graisseuse): dose initiale: 7.5 à 15 mg chez les nourrissons, 4.5 mg/kg chez les enfants plus âgés; 2e jour: réduire la dose à la moitié de la dose initiale; 3e jour: réduire la dose à un quart de la dose initiale
- état de mal asthmatique: dose initiale: 7.5 à 15 mg en bolus, puis 0.15 à 0.3 mg/kg par jour
- poussées aiguës de dermatoses sévères (p.ex. œdème de Quincke, pemphigus vulgaire, eczémas non contrôlables, sarcoïdose cutanée): posologie selon la gravité: dose élevée de 0.3 à 0.45 mg/kg par jour; dose moyenne de 0.15 mg/kg par jour; dose d’entretien de 0.04 mg/kg par jour
- hémopathies aiguës (p.ex. anémie hémolytique aiguë): selon la gravité de la maladie: 6.5 à 40 mg/m2 de surface corporelle pendant 4 à 5 jours tous les 28 jours
- insuffisance corticosurrénalienne primaire et secondaire aiguë (si l’hydrocortisone n’est pas disponible; toutefois uniquement lors de traitement concomitant par un minéralocorticoïde): dose initiale: 7.5 à 15 mg chez les nourrissons, 4.5 mg/kg chez les enfants plus âgés; puis passer à l’hydrocortisone
- prophylaxie et traitement des vomissements induits par des cytostatiques: 8 mg/m2 de surface corporelle environ 30 min. avant la chimiothérapie, puis 16 mg/m2 en 2 à 4 doses partielles distribuées dans la journée
Traitement de la COVID-19:
Patients présentant des troubles de la fonction hépatique
Aucun ajustement de la posologie n’est nécessaire.
Patients présentant des troubles de la fonction rénale
Aucun ajustement de la posologie n’est nécessaire.
Patients âgés
Aucun ajustement de la posologie n’est nécessaire.
Enfants et adolescents
Pour les patients pédiatriques (adolescents à partir de 12 ans et plus), une dose de 6 mg par voie intraveineuse une fois par jour durant une période allant jusqu’à 10 jours est recommandée. La durée du traitement dépend de la réponse clinique et des besoins individuels du patient. Seulement des données limitées sont disponibles pour les patients âgés de moins de 18 ans.
Contre-indications
Dans des situations dans lesquelles l’administration de glucocorticoïdes peut sauver la vie du patient, une administration aiguë ne présente aucune contre-indication.
Ne pas utiliser ce médicament en cas d’hypersensibilité à l’un des composants.
Une injection intra-articulaire est contre-indiquée dans les cas suivants:
- infection de l’articulation ou des régions avoisinantes
- arthrite bactérienne
- instabilité articulaire
- tendance hémorragique (hémorragies spontanées ou liées à une thérapie anticoagulante)
- calcification péri-articulaire
- ostéonécrose avasculaire
- rupture du tendon
- articulation de Charcot
En cas d’infections au site d’injection, une infiltration sans traitement causal supplémentaire est contre-indiquée.
Mises en garde et précautions
Le traitement par Dexaméthasone Galepharm peut provoquer une immunosuppression et ainsi accroître le risque d’infections bactériennes, virales, fongiques, parasitaires et opportunes. De plus, Dexaméthasone Galepharm est susceptible de masquer les symptômes d’une infection existante ou en développement et ainsi d’en entraver le diagnostic. Des infections latentes, y compris tuberculose ou hépatite B, peuvent être réactivées.
Comme toute glucocorticothérapie, le traitement par Dexaméthasone Galepharm ne doit pas être interrompu soudainement, mais en réduisant la dose journalière lentement et progressivement afin d’éviter une aggravation ou une reprise aiguë de la maladie, une insuffisance corticosurrénalienne aiguë et un syndrome de sevrage de la cortisone.
Chez les COVID-19 patients déjà traités pour d’autres raisons par des corticostéroïdes systémiques (oraux) (p.ex. des patients atteints de bronchopneumopathie chronique obstructive), mais qui ne nécessitent pas d’apport d’oxygène supplémentaire, les corticostéroïdes systémiques ne doivent pas être arrêtés.
La prudence est de mise en cas de:
- infections virales aiguës (hépatite B, varicelle, zona, Herpes simplex, kératite herpétique, poliomyélite, rougeole). Il convient d’être particulièrement prudent si, pendant un traitement par Dexaméthasone Galepharm, des patient(e)s immunodéprimé(e)s sans antécédents de varicelle ou de rougeole sont en contact avec des personnes atteintes de ces maladies. L’évolution de ces maladies chez des patients sous traitement par Dexaméthasone Galepharm peut être particulièrement grave. La varicelle survenant durant un traitement systémique par des corticostéroïdes peut revêtir une forme dont l’évolution est grave et dont l’issue peut être mortelle, en particulier chez l’enfant. Elle nécessite un traitement immédiat, p.ex. par aciclovir i.v. Chez les patients à risque, l’administration d’aciclovir à titre prophylactique ou une immunoprophylaxie passive par administration d’immunoglobuline du virus varicelle-zona sont indiquées
- infections bactériennes aiguës et chroniques: administrer uniquement sous protection antibiotique. Une amibiase latente doit être exclue avant le traitement et les patients atteints de tuberculose latente ou de tuberculose d’organe doivent recevoir des tuberculostatiques à titre prophylactique pendant un traitement à long terme par glucocorticoïdes
- mycoses et parasitose systémiques. Chez les patients présentant une infestation connue ou présumée par des strongyloïdes, les glucocorticoïdes peuvent entraîner des récidives ou le développement de la maladie
- environ 8 semaines avant et 2 semaines après une vaccination préventive par des vaccins vivants. Les vaccinations avec des vaccins inactivés sont en principe possibles. Il faut cependant considérer que la réaction immune et ainsi le succès de la vaccination peuvent être diminués en cas de posologies plus élevées de glucocorticoïdes
- lymphadénite à la suite de vaccination par le BCG
- hépatite chronique, HBsAg-positive
- diabète sucré difficile à contrôler, la tolérance au glucose pouvant être diminuée. Des contrôles sanguins doivent être effectués régulièrement et la dose d’antidiabétiques doit, le cas échéant, être ajustée
- hypothyroïdie et cirrhose du foie car, dans de tels cas, l’effet des glucocorticoïdes est renforcé
- tendance à la thrombose
- infarctus du myocarde récent
- hypertension et insuffisance cardiaque difficile à contrôler
- myasthénie et administration concomitante d’inhibiteurs de la cholinestérase car, dans de tels cas, l’effet des inhibiteurs de la cholinestérase est diminué et le risque de crise myasthénique est accru (le traitement par des inhibiteurs de la cholinestérase devrait être interrompu, dans la mesure du possible, 24 heures avant l’administration d’un corticostéroïde)
- ulcère gastro-intestinal
- ostéoporose
- maladies psychiatriques, y compris comportement suicidaire (même anamnestique): une surveillance neurologique ou psychiatrique est conseillée
- glaucome à angle ouvert ou fermé, ulcères ou lésions cornéens: une surveillance ophtalmologique étroite et un traitement sont conseillés
A cause du risque de perforation intestinale, Dexaméthasone Galepharm ne peut être utilisé que pour des indications impératives et sous une surveillance adéquate en cas de:
- colite ulcéreuse grave sans irritation péritonéale, accompagnée d’un risque de perforation
- diverticulite
- entéro-anastomoses (en phase postopératoire immédiate)
Les symptômes d’une irritation péritonéale à la suite d’une perforation gastro-intestinale peuvent être absents chez les patients recevant des doses élevées de glucocorticoïdes.
En cas d’utilisation concomitante de fluoroquinolones, il existe un risque accru d’atteintes des tendons, de ténosites et de ruptures des tendons.
Une augmentation temporaire de la dose journalière de corticoïdes peut s’avérer nécessaire pendant les situations de stress physique.
Des réactions anaphylactiques graves peuvent survenir et nécessiter des mesures de précaution appropriées (être prêt à traiter un choc anaphylactique).
En cas de doses élevées, un apport suffisant de potassium et une restriction de sodium doivent être observés. De plus, le taux sérique de potassium doit être surveillé.
En cas de doses élevées, une bradycardie peut survenir.
En cas d’administration locale, il faut faire attention à la survenue éventuelle d’effets indésirables et d’interactions systémiques.
L’administration par voie intra-articulaire de glucocorticoïdes augmente le risque d’infections articulaires. Une administration à long terme ou répétée de glucocorticoïdes dans des articulations portantes peut entraîner le renforcement de symptômes d’usure.
Après l’utilisation de la dexaméthasone seule ou en association avec des médicaments chimiothérapeutiques, un syndrome de lyse tumorale (SLT) a été rapporté chez des patients avec des maladies hématologiques malignes. Les patients avec des tumeurs à forte vitesse de prolifération ou à haute sensibilité envers les principes actifs cytotoxiques ainsi que les patients avec une charge tumorale élevée courent un risque important de développer un SLT et doivent donc être surveillés étroitement. En outre, des mesures de précaution correspondantes doivent être prises.
Crise de phéochromocytome
Après l’utilisation de corticoïdes, la survenue d’une crise de phéochromocytome pouvant être fatale a été rapportée. Chez les patients avec un phéochromocytome supposé ou diagnostiqué, les corticoïdes ne doivent être utilisés qu’après une évaluation adéquate des risques et des bénéfices. Si de potentiels symptômes d’une crise de phéochromocytome, tels qu’une crise hypertensive, une insuffisance cardiaque, de la tachycardie, des maux de tête, des douleurs abdominales et/ou thoraciques, surviennent chez un patient traité par des corticostéroïdes, la possibilité d’un phéochromocytome inconnu jusque-là doit être envisagée.
Troubles visuels
Des troubles visuels peuvent survenir lors d’un traitement systémique ou local par des corticostéroïdes. Si des symptômes tels qu’une vision floue ou d’autres troubles visuels surviennent, il convient d’adresser le patient à un ophtalmologue pour clarifier les causes potentielles, telles que cataracte, glaucome ou d’autres maladies rares comme la choriorétinopathie séreuse centrale, survenues lors du traitement local ou systémique par des corticostéroïdes.
Prématurés
Après un traitement précoce (< 96 heures après la naissance) chez les prématurés avec maladie pulmonaire chronique à une posologie initiale de 0.25 mg/kg deux fois par jour, les données disponibles indiquent des effets négatifs à long terme concernant le développement neuronal.
Cardiomyopathie hypertrophique
Des cas de cardiomyopathie hypertrophique ont été rapportés après administration systémique de corticostéroïdes, y compris de dexaméthasone, à des prématurés. Dans la majorité des cas rapportés, cette cardiomyopathie était réversible après l’arrêt du traitement. Chez les prématurés recevant un traitement systémique par dexaméthasone, une évaluation diagnostique et une surveillance de la fonction et de la structure cardiaques doivent être effectuées (voir «Effets indésirables»).
Enfants et adolescents
Dexaméthasone Galepharm ne devrait être administré durant la phase de croissance de l’enfant qu’après une évaluation soigneuse des bénéfices par rapport aux risques. Le traitement doit être administré soit de manière intermittente, soit de manière alternante.
Patients âgés
Comme les patients âgés présentent un risque accru d’ostéoporose, Dexaméthasone Galepharm ne doit être administré qu’après une évaluation soigneuse des bénéfices par rapport aux risques.
Excipients
Sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ml, c.-à-d. qu’il est essentiellement «sans sodium».
Propylène glycol
Dexaméthasone Galepharm Amp: 4 mg/1 ml contient 20 mg de propylène glycol par 1 ml, correspondant 20 mg/ml.
Dexaméthasone Galepharm Amp: 8 mg/2 ml contient 40 mg de propylène glycol par 2 ml, correspondant 20 mg/ml.
L’administration concomitante avec n’importe quel substrat pour l’alcool déshydrogénase comme l’éthanol peut induire des effets indésirables graves chez les nouveau-nés.
Interactions
| Médicament | Modification de l’effet |
| Salurétiques, amphotéricine, laxatifs | Augmentation de l’excrétion de potassium |
| Médicaments inducteurs du CYP3A4 tels que: rifampicine, phénytoïne, carbamazépine, barbituriques et primidon | Diminution de l’effet des corticoïdes par augmentation de la clairance |
| Médicaments inhibiteurs du CYP3A4 tels que: kétoconazol, itraconazol, ritonavir et cobicistat | Le risque d’effets indésirables systémiques des corticoïdes peut être augmenté |
| Ephédrine | Diminution de l’effet par accélération du métabolisme des corticoïdes |
| Antiphlogistiques non stéroïdiens/antirhumatismaux non stéroïdiens | Risque accru d’hémorragies, d’ulcérations et de perforations gastro-intestinales |
| Salicylés | Diminution de l’effet des salicylés par augmentation de la clairance. En cas de traitement à long terme: risque accru d’hémorragies et d’ulcérations gastro-intestinales pouvant aller jusqu’à la perforation. Une réduction de la dose de glucocorticoïdes doit être faite avec précaution car des intoxications aux salicylés peuvent survenir. |
| Œstrogènes | Renforcement possible de l’effet des corticoïdes par diminution de la clairance |
| Vaccination par vaccins inactivés | Limitation possible de l’immunisation |
| Inhibiteurs de la cholinestérase | Diminution de l’inhibition de la cholinestérase |
| Glycosides cardiaques | Renforcement de l’effet des glycosides par manque de potassium |
| Antidiabétiques oraux, insuline | Réduction de la baisse du sucre; besoin éventuellement accru en antidiabétiques |
| Dérivés de la coumarine | Affaiblissement ou renforcement de l’effet anticoagulant; un ajustement de la dose d’anticoagulant peut s’avérer nécessaire en cas d’utilisation concomitante |
| Praziquantel | Abaissement possible de la concentration de Praziquantel dans le sang |
| Atropine et autres anticholinergiques | Risque d’élévation encore plus grande d’une pression intraoculaire déjà élevée |
| Inhibiteurs de l’ECA | Risque accru de modifications de l’hémogramme |
| Chloroquine, hydroxychloroquine, méfloquine | Risque accru de myopathies et de cardiomyopathies |
| Immunosuppresseurs | Prédisposition accrue aux infections et possible manifestation ou aggravation d’infections latentes existantes. |
| Ciclosporine | De plus, risque accru de crises convulsives par augmentation du taux sanguin de ciclosporine |
| Myorelaxants non dépolarisants | Prolongation éventuelle de la relaxation musculaire |
| Protiréline | Amoindrissement possible de l’élévation de TSH |
| Fluoroquinolones | Risque éventuellement accru d’atteintes des tendons |
Grossesse, allaitement
Grossesse
Des expérimentations animales ont montré des effets indésirables chez le fœtus; il n’existe aucune étude contrôlée chez la femme enceinte. Comme tous les glucocorticoïdes, la dexaméthasone traverse elle aussi la barrière placentaire. En cas de traitement à long terme durant la grossesse, des troubles de croissance intra-utérine, par exemple, ne peuvent être exclus. Un traitement en fin de grossesse expose le fœtus au risque d’une atrophie des glandes corticosurrénales pouvant exiger un traitement de substitution diminuant progressivement chez le nouveau-né.
C’est pourquoi Dexaméthasone Galepharm, comme tous les glucocorticoïdes, ne doit pas être administré pendant la grossesse, et en particulier au cours du premier trimestre, sauf en cas de nécessité absolue. En cas d’indication établie, la prednisolone (ou prednisone) est préférable à tous les autres glucocorticoïdes, particulièrement aux glucocorticoïdes fluorés, son passage dans le placenta étant le plus faible.
En cas de grossesse présumée ou confirmée, le médecin doit absolument être informé.
Les enfants dont la mère a été traitée avec des doses élevées de glucocorticoïdes durant la grossesse doivent être surveillés soigneusement pour détecter tout symptôme d’hypocorticisme.
Des études ont montré qu’il existe un risque accru d’hypoglycémie néonatale après une administration prénatale de courte durée de corticostéroïdes (y compris de dexaméthasone) à des femmes enceintes présentant un risque d’accouchement prématuré tardif.
Allaitement
La dexaméthasone, comme tous les autres glucocorticoïdes, se retrouve en très faibles quantités dans le lait maternel et pourrait entraver, entre autres, la fonction corticosurrénalienne et la croissance du nourrisson. C’est pourquoi, les mères recevant des glucocorticoïdes pendant l’allaitement doivent arrêter d’allaiter.
Effet sur l’aptitude à la conduite et l’utilisation de machines
La capacité à conduire un véhicule et à manipuler des machines peut être altérée, particulièrement au début du traitement par Dexaméthasone Galepharm. Ces perturbations s’expliquent surtout par des altérations de l’humeur, de la prise d’initiative et de la capacité de concentration.
Effets indésirables
Les effets indésirables de la dexaméthasone dépendent de la dose et de la durée du traitement ainsi que de l’âge, du sexe et de la maladie de base du patient.
Le risque d’effets indésirables est faible lors de corticothérapie de courte durée. On surveillera cependant les hémorragies intestinales (souvent liées au stress), dont les symptômes peuvent être atténués par l’administration de corticoïdes.
Lors de traitement prolongé à doses élevées, les effets secondaires connus des glucocorticoïdes peuvent survenir.
Infections et infestations
Augmentation du risque d’infections, masquage d’infections, survenue, aggravation ou réactivation d’infections bactériennes, virales, fongiques, parasitaires et opportunes, activation d’une strongyloïdose.
Affections hématologiques et du système lymphatique
Leucocytose modérée, lymphopénie, éosinopénie, polycythémie.
Affections du système immunitaire
Réactions d’hypersensibilité, réactions anaphylactiques sérieuses telles que: arythmies, bronchospasme, élévation ou baisse de la pression artérielle, arrêt circulation, arrêt cardiaque.
En cas d’injection locale, d’éventuels effets indésirables et interactions systémiques doivent être surveillés.
Affections endocriniennes
Insuffisance corticosurrénalienne.
Déclenchement d’une crise de phéochromocytome chez des patients présentant un phéochromocytome préexistant (également latent).
Syndrome de Cushing (p.ex. faciès lunaire, obésité du tronc), voir «Mises en garde et précautions».
Troubles du métabolisme et de la nutrition
Rétention du sodium accompagnée de formation d’œdèmes, excrétion accrue de potassium, calcium et phosphate.
Prise pondérale, diminution de la tolérance au glucose, diabète sucré, hypercholestérolémie, hypertriglycéridémie, augmentation de l’appétit.
Affections psychiatriques
Psychose, manie, dépression, hallucinations, labilité affective, irritabilité, augmentation de la prise d’initiative, euphorie, agitation intérieure, troubles du sommeil, comportement suicidaire.
Affections du système nerveux
Elévation de la pression intracrânienne accompagnée de stase papillaire (pseudotumeur cérébrale), apparition ou aggravation de l’épilepsie (convulsions).
Affections oculaires
Augmentation de la pression intraoculaire (glaucome), opacification du cristallin (cataracte), avec en particulier une opacification sous-capsulaire postérieure, aggravation des symptômes en cas d’ulcères cornéens, favorise les infections oculaires virales, fongiques et bactériennes, aggravation des infections cornéennes bactériennes, ptose, mydriase, chémosis, perforation sclérale iatrogène, rarement exophtalmie réversible. De plus, en cas d’administration sous-conjonctivale: kératite (causé par le virus Herpex simplex) de même que perforations cornéennes lors de kératite, choriorétinopathie, vision floue.
Affections cardiaques
Cardiomyopathie hypertrophique chez les prématurés (voir «Mises en garde et précautions»).
Affections vasculaires
Hypertension.
Risque accru d’artériosclérose et de thrombose, vasculite, augmentation de la fragilité des capillaires sanguins.
Affections gastro-intestinales
Ulcères peptiques gastriques et duodénaux, hémorragies de l’estomac, pancréatite, troubles de l’estomac.
Affections de la peau et du tissu sous-cutané
Vergetures (striae rubrae), dermatite péri-orale, atrophie cutanée, hémorragies cutanées punctiformes (pétéchies), hématomes (ecchymoses), acné stéroïdienne, retard de cicatrisation, télangiectasies, hypertrichose, modification de la pigmentation cutanée.
Affections musculosquelettiques et du tissu conjonctif
Atrophie musculaire, faiblesse musculaire, myopathie, atteintes des tendons, ténosite, rupture des tendons, ostéoporose, ostéonécrose aseptique, retard de croissance chez l’enfant, lipomatose épidurale.
Affections des organes de reproduction et du sein
Troubles de la sécrétion des hormones sexuelles (aménorrhée, pilosité anormale, impuissance).
Troubles généraux et anomalies au site d’administration
Retard de cicatrisation. La répétition de l’administration intramusculaire, intra-articulaire et sous-lésionnelle de dexaméthasone (ou d’un autre glucocorticoïde) peut entraîner des dommages tissulaires locaux graves (pouvant aller jusqu’à des atrophies et des nécroses).
L’annonce d’effets secondaires présumés après l’autorisation est d’une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d’effet secondaire nouveau ou grave via le portail d’annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
Surdosage
La toxicité aiguë des glucocorticoïdes étant faible, des intoxications induites par un surdosage aigu de glucocorticoïdes n’ont été que rarement observées jusqu’à présent. En cas de surdosage chronique, il faut s’attendre à un renforcement des effets indésirables qui influencent particulièrement le système endocrinien, le métabolisme et l’équilibre électrolytique. En cas de surdosage, il n’existe aucun antidote spécifique et le traitement est symptomatique.
Propriétés/Effets
Code ATC
H02AB02
Mécanisme d’action
Le mécanisme d’action des glucocorticoïdes est complexe.
La dexaméthasone se lie à des récepteurs intracellulaires et les active. Le complexe glucocorticoïde-récepteurs activé migre dans le noyau cellulaire où il initie ou bloque la synthèse de certaines protéines en se fixant à des sites spécifiques de liaison à l’ADN.
- Les protéines dont la synthèse est initiée incluent, entre autres, la lipocortine 1 qui inhibe la phospholipase A2, importante pour une réaction inflammatoire, et l’enzyme de conversion de l’angiotensine (ECA), intervenant dans le circuit de régulation de la pression artérielle
- Les protéines dont la synthèse est inhibée incluent différentes cytokines (p.ex. TNF-alpha, interleukine-2, interleukine-6) qui activent les cellules du système immunitaire, et diverses enzymes pro-inflammatoires (p.ex. collagénase). L’induction de la NO-synthétase de même que celle de la cyclo-oxygénase sont également inhibées
En plus de ces mécanismes génomiques qui interviennent avec un temps de latence compris entre une demi-heure et plusieurs heures, il existe quelques effets rapides en partie observés dès faible concentration plasmatique (p.ex.: suppression de la sécrétion endogène de cortisol) et d’autres effets seulement présents à des concentrations plus élevées (p.ex. stabilisation membranaire). Le mécanisme le plus probable de ces derniers est l’incorporation de glucocorticoïdes dans la membrane cellulaire comme événement initial.
Pharmacodynamique
La dexaméthasone exerce une action anti-inflammatoire, antiallergique (anti-œdémateuse) et immunosuppressive puissante. Elle accélère le métabolisme des glucides, a des effets antitoxiques non spécifiques (protection membranaire) et favorise la microcirculation (stabilisation de l’irrigation cérébrale).
La dexaméthasone présente un très faible effet minéralocorticoïde.
L’équivalence des doses anti-inflammatoires de dexaméthasone et d’autres glucocorticoïdes est la suivante: 1 mg de dexaméthasone = 6 mg de triamcinolone ou méthylprednisolone = 7.5 mg de prednisone ou prednisolone = 30 mg d’hydrocortisone = 35 mg de cortisone.
Efficacité clinique
Comme d’autres glucocorticoïdes, la dexaméthasone est utilisée pour un large éventail d’indications. En raison de sa longue demi-vie biologique, la dexaméthasone est particulièrement indiquée pour les indications pour lesquelles un effet glucocorticoïde continu est souhaité. Pour quelques indications, la dexaméthasone est préférentiellement choisie en raison de son faible effet minéralocorticoïde.
Pour le traitement de la COVID-19
RECOVERY (Randomised Evaluation of COVid-19 thERapY), une étude basée sur une plateforme, à l’initiative de la recherche, randomisée individuellement, contrôlée, ouverte, adaptative, est une étude d’évaluation de l’effet de différents traitements sur des patients qui sont soignés dans un hôpital en raison de la COVID-19.
L’étude a été réalisée dans 176 hôpitaux au Royaume-Uni.
6425 patients ont reçu soit de la dexaméthasone (2104 patients) soit le traitement standard habituel (4321 patients) en fonction de leur randomisation. Une infection à SARS-CoV-2 avait été confirmée par des analyses chez 89% des patients.
Lors de la randomisation, 16% des patients étaient déjà sous ventilation mécanique invasive ou sous oxygénothérapie par membrane extracorporelle, 60% étaient sous oxygène seul (avec ou sans ventilation non invasive) et 24% ne recevaient pas d’assistance respiratoire.
Les patients étaient âgés de 66.1 +/- 15.7 ans en moyenne. 36% des patients étaient de sexe féminin. 24% des patients avaient des antécédents de diabète, 27% étaient atteints de maladies cardiovasculaires et 21% d’une affection pulmonaire chronique.
Critère d’évaluation primaire
Le taux de mortalité à 28 jours a été statistiquement réduit dans le groupe dexaméthasone avec 482 décès sur 2104 patients (22.9%) par rapport au groupe de traitement standard avec 1110 décès sur 4321 patients (25.7%) (rapport des taux [rate ratio, RR]: 0.83; intervalle de confiance à 95% [IC]: 0.75-0.93; p < 0.001).
Dans le groupe dexaméthasone, la mortalité chez les patients sous ventilation mécanique invasive (29.3% vs. 41.4%; RR: 0.64; IC95%: 0.51-0.81) et chez les patients sous oxygène supplémentaire sans ventilation mécanique invasive (23.3% vs. 26.2%; RR: 0.82; IC95%: 0.72-0.94), était inférieure à celle du groupe de traitement standard.
Aucun effet manifeste de la dexaméthasone n’a été observé chez les patients ne recevant pas d’assistance respiratoire lors de la randomisation (17.8% vs. 14.0%; RR: 1.19; IC95%: 0.91-1.55).
Critères d’évaluation secondaires
La durée d’hospitalisation a été plus courte (médiane de 12 jours vs. 13 jours) et la probabilité de sortie au cours des 28 jours après randomisation a été plus élevée (RR: 1.10; IC95%: 1.03-1.17) pour les patients du groupe dexaméthasone que pour ceux du groupe de traitement standard.
En accord avec le critère d’évaluation primaire, l’effet le plus important sur la sortie de l’hôpital dans les 28 jours a été observé chez les patients sous ventilation mécanique invasive après la randomisation (RR: 1.48; IC95%: 1.16-1.90), suivis par le groupe sous oxygène seul (RR: 1.15; IC95%: 1.06-1.24). Aucun effet positif n’a été observé chez les patients n’ayant pas reçu d’oxygène (RR: 0.96; IC95%: 0.85-1.08).
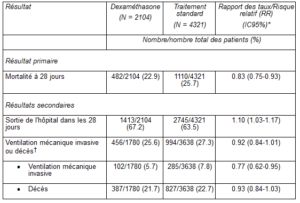
* Les RR ont été ajustés sur l’âge en ce qui concerne les résultats de la mortalité à 28 jours et la sortie de l’hôpital. Les RR ont été ajustés sur l’âge en ce qui concerne le résultat de la ventilation mécanique invasive reçue ou du décès et de leurs sous-composants.
† Les patients qui recevaient déjà une ventilation mécanique invasive lors de la randomisation ont été exclus de cette catégorie.
Sécurité
Quatre événements indésirables graves (SAE) liés au traitement de l’étude sont survenus: deux SAE d’hyperglycémie, un SAE de psychose induite par des stéroïdes et un SAE de saignement gastro-intestinal supérieur.
Analyse des sous-groupes
Effets de l’attribution au groupe dexaméthasone sur la mortalité à 28 jours, en fonction de l’âge et de l’assistance respiratoire randomisée reçue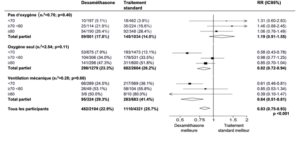
Effets de l’attribution au groupe dexaméthasone sur la mortalité à 28 jours, en fonction de l’assistance respiratoire randomisée reçue et des antécédents d’affection chronique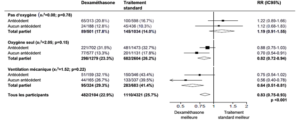
Pharmacocinétique
Absorption
Après injection intraveineuse de dexaméthasone-21-dihydrogène phosphate, l’hydrolyse de l’ester s’effectue très rapidement. Chez l’homme, le pic sanguin de dexaméthasone libre sous sa forme alcoolique est atteint 10 minutes après l’injection de l’ester. La dexaméthasone-21-dihydrogène phosphate injectée par voie intramusculaire est résorbée rapidement et quasi totalement en cas d’irrigation sanguine normale, le pic sanguin étant atteint 60 minutes après l’injection i.m. L’effet pharmacologique maximal se manifeste toutefois avec un délai (environ 2 heures après l’injection) et persiste au-delà de la demi-vie plasmatique.
Distribution
A la suite de l’application intraveineuse de dexaméthasone-21-dihydrogène phosphate, le pic de dexaméthasone dans le liquide céphalo-rachidien est atteint au bout de 4 heures et représentent environ un sixième de la concentration plasmatique concomitante. La chute du taux de dexaméthasone dans le liquide céphalo-rachidien ne se fait que lentement, si bien qu’environ deux tiers de la concentration maximale sont encore présents 24 heures après l’injection.
La dexaméthasone se lie, de manière dose-dépendante et jusqu’à environ 80 %, aux protéines plasmatiques, surtout à l’albumine plasmatique. En cas de doses très élevées, la majeure partie circule sous forme libre dans le sang, c’est-à-dire sans être liée à des protéines.
Le volume de distribution de dexaméthasone est de 0.6 à 0.8 l/kg.
En cas d’hypoalbuminémie, la proportion de corticoïdes non liés (actifs) augmente.
La dexaméthasone franchit aussi bien la barrière hémato-encéphalique que la barrière placentaire et passe dans le lait maternel.
Métabolisme
La dexaméthasone est éliminée principalement sous forme inchangée par les reins. Chez l’homme, seule une petite partie subit une hydrogénation ou une hydroxylation de la molécule, les métabolites principaux étant alors la 6-hydroxydexaméthasone et la 20-dihydrodexaméthasone. 30 à 40 % des molécules de dexaméthasone se lient à l’acide glucuronique ou à l’acide sulfurique dans le foie humain et se retrouvent sous cette forme dans l’urine.
Elimination
La demi-vie d’élimination plasmatique de la dexaméthasone est de 3 à 5 heures, mais sa demi-vie biologique est considérablement plus longue, atteignant 36 à 72 heures. Chez l’adulte, la clairance plasmatique est de 2 à 5 ml/min/kg. Après infiltration locale et injection intra-articulaire à la dose de 4 ou 8 mg, la dexaméthasone est totalement éliminée après 4 à 10 jours en moyenne en cas d’irrigation normale du site d’injection.
Cinétique pour certains groupes de patients
Pendant la grossesse, la demi-vie d’élimination est prolongée.
Troubles de la fonction hépatique
En cas de maladie hépatique grave (p.ex. hépatite, cirrhose du foie) et en cas d’hypothyroïdie, la demi-vie d’élimination est prolongée.
Troubles de la fonction rénale
Atteintes rénales: pas de modifications essentielles de l’élimination.
Enfants et adolescents
Chez les nouveau-nés, la clairance plasmatique est plus faible que chez les enfants et les adultes.
Données précliniques
Les glucocorticoïdes présentent une toxicité aiguë très faible.
Toxicité à long terme (ou toxicité en cas d’administration répétée)
Il n’existe aucune donnée sur la toxicité chronique chez l’homme et chez l’animal.
Mutagénicité
L’effet mutagène de la dexaméthasone n’a pas été suffisamment étudié. Il existe des indications provisoires d’un potentiel mutagène dont l’importance n’a pas été établie à ce jour.
Carcinogénicité
Des expérimentations animales au long cours ne sont pas disponibles.
Toxicité sur la reproduction
En expérimentation animale chez les souris, les rats, les hamsters, les lapins et les chiens, la dexaméthasone provoque des fentes palatines et, dans une moindre mesure, d’autres malformations.
Remarques particulières
Incompatibilités
Dexaméthasone Galepharm Amp ne doit pas être mélangé avec d’autres médicaments. En ce qui concerne la compatibilité avec des solutions pour perfusion, voir «Remarques concernant la manipulation».
Influence sur les méthodes de diagnostic
Tests d’allergie
Les réactions cutanées peuvent être atténuées.
Taux sériques
Diminués: VS, temps de coagulation (Lee White), acide urique, testostérone, potassium, TSH, thyroxine, T3.
Augmentés: glucose, cholestérol, sodium, chlorure.
Taux urinaires
Diminués: 17-cétostéroïdes.
Augmentés: créatinine, calcium, glucose (en cas de prédisposition).
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques particulières concernant le stockage
Ne pas conserver au-dessus de 25 °C. Ne pas conserver au réfrigérateur. Ne pas congeler.
Conserver le récipient dans l’emballage d’origine pour le protéger de la lumière. Tenir hors de portée des enfants.
Remarques concernant la manipulation
Compatibilités avec des solutions pour perfusion
Dexaméthasone Galepharm Amp doit être appliqué si possible directement par voie intraveineuse ou injecté dans le tube de perfusion.
Dexaméthasone Galepharm Amp est compatible avec les solutions pour perfusion suivantes et destiné à être utilisé dans les 24 heures: solution saline isotonique et solution de glucose à 5 %.
Lors d’association avec des solutions pour perfusion, les informations des fournisseurs respectifs sur leurs solutions pour perfusion de même que sur la compatibilité, les contre-indications, les effets indésirables et les interactions doivent être respectées.
Numéro d’autorisation
66710 (Swissmedic)
Présentation
Dexaméthasone Galepharm Amp 4 mg/1 ml, solution injectable: 3 ou 10 ampoules à 1 ml. (B)
Dexaméthasone Galepharm Amp 8 mg/2 ml, solution injectable: 3 ou 10 ampoules à 2 ml. (B)
Titulaire de l’autorisation
Galepharm AG, Zürich.
Mise à jour de l’information
Juin 2022.